مقدمه
متاستاز در اندام های حیاتی مانند ریه و مغز، مسئول بیش از 90 درصد از کل مرگ و میر سرطان در کلینیک است. شیمیدرمانیها در برابر متاستاز اغلب با شکست مواجه میشوند. زیرا عوامل سیتوتوکسیک میتوانند مکانیسمهای متعددی (به عنوان مثال، ترشح واسطههای پیشالتهابی) برای تسهیل تشکیل متاستاز را القا کنند. اگرچه با جراحی برداشته میشود. اما میکروتومورهای باقی مانده سرسخت می توانند به راحتی باعث عود و متاستاز شوند. که منجر به پیش آگهی بسیار ضعیف برای بیماران می شود. (این مطلب توسط پژوهشگران دارویی در مرکز تحقیقات صنعتی نیکاپویش تولید و ارائه میشود.)
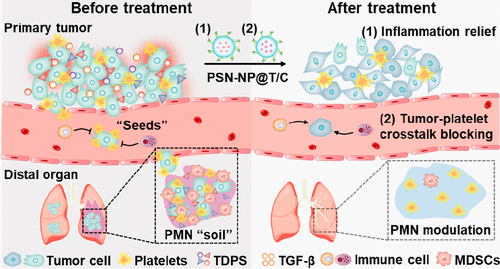
مهار هدفمند التهاب تومور و تداخل تومور-پلاکت توسط دارورسانی با واسطه نانوذرات متاستاز، باعث کاهش سرطان میشود.
پژوهشگران دارویی معتقدند، آبشار متاستاز از آزادسازی «seeds» سلول تومور پرو متاستاتیک از تومورهای اولیه آغاز میشود. و به دنبال آن، بقای آنها در گردش خون و نشست «seeds» در «soil» بارور شده از طاقچههای پیشمتاستاتیک (PMN) در اندامهای دوردست است. التهاب در اندام های ثانویه یک محرک و مشخصه ضروری برای توسعه soil PMN است. soil PMN التهابی نابهنجار توسط تومورهای اولیه تولید می شود.
که ترشحات متاستاتیکی را آزاد می کند. و نفوذپذیری عروقی را افزایش می دهد و سلول های سرکوبگر مشتق از میلوئید (MDSCs) را به خدمت می گیرد. و بستری ایده آل برای کلون سازی “seeds” فراهم می کند. علاوه بر این، شواهد در حال ظهور نقش حیاتی پلاکت ها را در پخش و بذردهی “seeds” نشان داده اند. در طول مهاجرت هماتوژن «seeds متاستاتیک»، پلاکتها میتوانند به سلولهای تومور در گردش (CTCs) کمک کنند. تا موانع کشندهای مانند نظارت ایمنی و نیروهای برشی را با تشکیل تودههای سلولی پلاکت-تومور دور بزنند.
و در نتیجه بقای آنها را تقویت کنند. علاوه بر این، کموکاینهای پیشالتهابی مانند لیگاند کموکاین 5 موتیف C-X-C CXCL5 که توسط پلاکتها ترشح میشوند. همچنین زیرمجموعهای از MDSCها را بهکار میگیرند تا طاقچههای پیشمتاستاتیک اولیه را تشکیل دهند. بنابراین «soil» را برای رشد «seeds» غنی میکنند. نکته مهم این است که هم التهاب و هم پلاکت ها با انتقال پاتولوژیک اپیتلیال- مزانشیمی (EMT)، فرآیندی که تغییر سلول های تومور اپیتلیال را به “seeds” پیش ساز مزانشیمی هماهنگ می کند، مرتبط هستند.
در نتیجه، سلول های تومور تهاجمی تر می شوند و یک آبشار متاستاتیک را آغاز می کنند. به طور موازی، ریزمحیط تومور التهابی پایدار میتواند با کسب ویژگیهای مشابه EMT و مقاومت، آپوپتوز را در سلولهای تومور تقویت کند. در حالی که پلاکتهای داخل توموری EMT را با ترشح مقادیر زیادی فاکتور رشد تبدیلکننده TGF-β β تسهیل میکنند. ، با هم یک “بزرگراه” برای “seeds” برای انتشار از نئوپلاسم اولیه به “soil” دوردست فراهم می کنند. همه این یافتهها التهاب تومور و پلاکتهای مرتبط با تومور را هدف بالقوهای برای کاهش متاستاز از طریق سرکوب همزمان گسترش «seeds» و تشکیل «soil» قرار دادهاند.
پلاکتهای فعال شده دارای پتانسیل زیادی برای ایجاد پلت فرم تحویل دارو، با میل طبیعی خود به سلولهای تومور هستند. گیرنده سطحی اینتگرین (به عنوان مثال، GPIIb/IIIa) می تواند به عنوان یک اپی توپ برای هدف قرار دادن پلاکت های فعال (از طریق آنتی بادی تک زنجیره ای ضد GPIIb/IIIa (scFv) یا پپتید RGD حلقوی) کار کند. علاوه بر این، نانوذرات دارای عوامل هدفگیری P-selectin (مانند فوکویدان و پپتید PSN) نتایج امیدوارکنندهای را در هدف قرار دادن پلاکتهای فعال نشان دادهاند، زیرا P-selectin به عنوان مشخصه بارز آنها توصیف شده است. هر دو سلکتین و اینتگرین از نظر عملکردی با ایجاد متاستاز مرتبط هستند.
با این حال، P-سلکتین بیشتر در میانجیگری تجمع تومور-پلاکتها، چرخاندن و اتصال سلولهای تومور (به ویژه CTCs) به اندوتلیوم نقش دارد. بنابراین، نانوذرات فعال شده پلاکتها بر اساس هدفگیری P-selectin نه تنها تومورهای اولیه و متاستاتیک را به دقت ردیابی میکنند، بلکه CTCها را از طریق یک پل پلاکتی نیز ردیابی میکنند.
 جمع بندی
جمع بندی
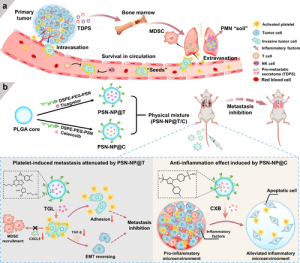
طی بررسی و تحقیقات پژوهشگران دارویی کاشت سلولهای بدخیم («seeds» متاستاز) برای پیوند مکانهای ثانویه، نیازمند یک طاقچه پیش متاستاتیک(PMN، soil متاستاز) مساعد است . پلاکت های مرتبط با التهاب و تومور (TAP) توسط تومورهای اولیه ربوده شده اند تا soil PMN را در اندام های دور ایجاد کنند. و همچنین انتشار “seeds” را تسهیل کنند. این مطالعه یک استراتژی ترکیبی با نانوذرات هدفگیری پلاکت فعال را گزارش میکند. تا فرآیند پویای کل متاستاز سرطان را هدف قرار دهد. که با مهار همزمان التهاب تومور و تداخل تومور-پلاکت، اثربخشی ضد متاستاز قوی را اعمال میکند. نتایج پژوهشگران دارویی نشان میدهد که اصلاح پپتید PSN (یک پپتید هدفدار P-سلکتین) تجمع نانوذرات را در تومور اولیه، PMN ریوی و متاستازها از طریق گرفتن پلاکتهای فعال شده غنی میکند.
براساس تحقیقات پژوهشگران دارویی؛ چنین ویژگی هایی با به تعویق انداختن پیشرفت انتقال اپیتلیال- مزانشیمی (EMT) در تومورها، به طور خاص مسدود کردن تداخل تومور-پلاکت برای حذف “سپر محافظ” پلاکت ها در اطراف “seeds” منتشر شده، به مهار موثر تقریباً در هر مرحله مهم و متوالی از آبشار متاستاز، و معکوس کردن ریزمحیط التهابی برای تداخل در تشکیل “soil” کمک می کند. این رویکرد متشکل از نانوذرات مهارکننده التهاب و مهارکننده TAP است. این رویکرد بهطور چشمگیری متاستازهای مختلف در ریه آبسکوپ را کاهش میدهد، از جمله متاستاز خودبخودی، متاستاز سلولهای تومور منتشر، و متاستاز پس از عمل.
این کار یک نانوپلتفرم قابل تعمیم از اختلال التهاب موازی و محاصره crosstalk تومور-TAP برای مقاومت در برابر تومورهای متاستاتیک ارائه میکند.

 جمع بندی
جمع بندی
بدون دیدگاه